Our Research
研究概要

細胞内PPI(Protein-Protein Interaction)の阻害による難治性疾患治療
難治性疾患を引き起こす原因として、人体を構成する細胞の情報伝達に中心的な役割を担っている
タンパク質間相互作用(PPI)が関わっていることが明らかとなってきました。
実際に、最近の医薬品売上高のTOP10では、細胞外のタンパク質間相互作用を阻害する抗体医薬が半分以上を占めており、
難治性疾患に有効性を示しています。

抗体医薬の仕組み
しかし、医薬品が生体内で起こる巨大なタンパク質同士の結合を阻害することを考えた場合、
抗体は細胞外においては有効ですが、細胞内においては作用を示すことが出来ません。
これは、抗体の大きさ(分子量)が15万程度で非常に大きく、細胞膜を透過できないことに起因しています。
そこで、細胞内で起こる多数のタンパク質間相互作用を阻害することに期待されるのが、細胞膜を透過することができる低分子化合物による創薬です。

低分子化合物と抗体の大きさ比較

難治性疾患を治療することを目指した低分子医薬品の探索技術
これまで、巨大なタンパク質(分子量3万~5万)の相互作用を、分子量500前後の低分子化合物で阻害することは難しいと考えられていました。 細胞内に浸透することができ、なおかつ標的とするタンパク質間相互作用を阻害することが可能な低分子化合物 の開発が求められています。
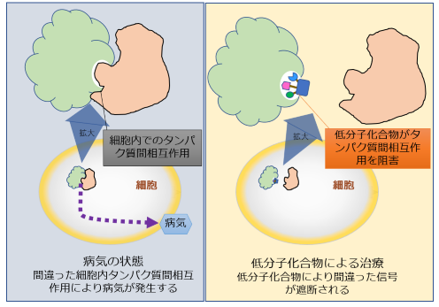
(左)疾患の原因となる細胞内でのタンパク質間相互作用
(右)当社技術による低分子化合物の作用
そこで、 弊社が着目しているのは、細胞内における天然変性タンパク質(Intrinsically Disordered Protein:IDP)と呼ばれるタンパク質です。
タンパク質間相互作用においては、長いひも状のIDP領域の限られた部分が、相手のタンパク質を認識する際に関与していることが知られています。
IDP領域は、 二次構造(ヘリックスやターン)を形成して、標的タンパク質を認識するため、
形成される二次構造を正確に模倣する低分子化合物であれば細胞内でPPIを阻害できると考えられます。
低分子化合物と抗体の大きさ比較
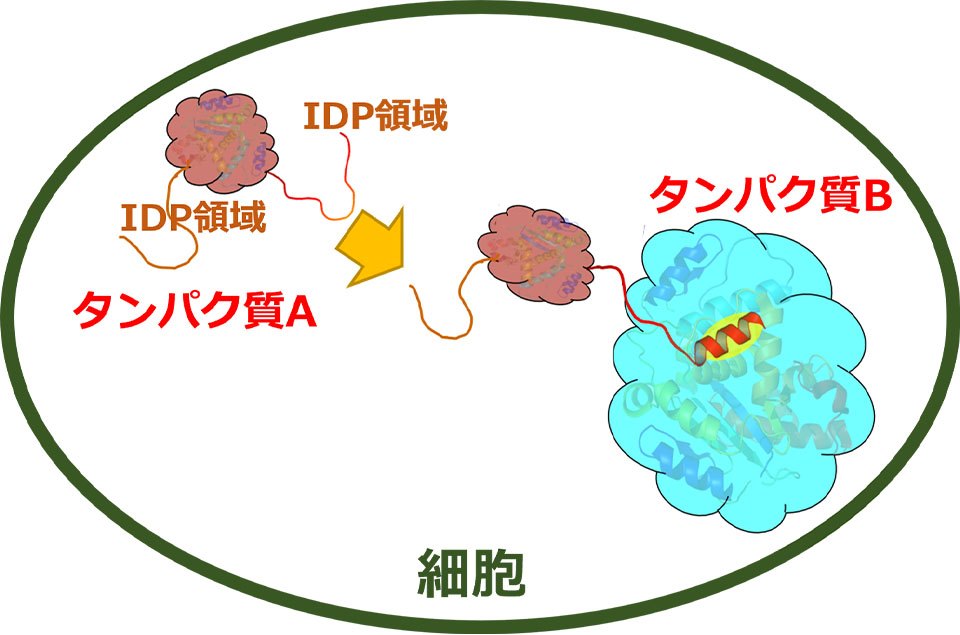
タンパク質Aの限られたIDP領域(ひも状)が二次構造を形成して相手のタンパク質Bを認識し結合する。

低分子化合物による細胞内PPI阻害
低分子化合物がIDPの結合構造を模倣してタンパク質Bに結合することにより、タンパク質Aは結合できない。
弊社の技術は、従来の低分子創薬で良く用いられている平面骨格ではなく、
立体的な籠型骨格を用いることでPPIに重要な3つのアミノ酸側鎖の位置を厳密に模倣する化合物デザインが行えることを特徴としています。

IDP模倣化合物(黄色)の例
弊社は製薬会社様やアカデミアとの共同研究により、核内受容体に選択的な阻害剤や、
がんの原因として手がつけられていないエリスロポエチンの阻害剤を取得しています。
細胞外にしか作用できない高分子医薬品では、難治性疾患治療の展開に限界があります。低分子化合物により細胞内PPIを阻害できることは、
これまでの研究結果でも明らかになってきており、低分子医薬品の開発による難治性疾患の治療には、大きな期待が寄せられています。
